
Reuters: Moderna, junto con la vacuna de Pfizer, que también ha demostrado tener una efectividad superior al 90% y en espera de más datos de seguridad y revisión regulatoria, EEUU podría tener dos vacunas autorizadas para uso de emergencia en diciembre con hasta 60 millones de dosis de vacunas disponibles para fin de año.
El próximo año, el gobierno de EEUU podría tener acceso a más de mil millones de dosis sólo de los dos fabricantes de vacunas, más de lo necesario para los 330 millones de habitantes del país.
Las vacunas, ambas construidas con nueva tecnología conocida como ARN mensajero o ARNm, representan nuevas y poderosas herramientas para combatir una pandemia que ha infectado a 54 millones de personas en todo el mundo y ha matado a 1,3 millones. La noticia también llega en un momento en que los casos de COVID-19 se están disparando, alcanzando nuevos récords en los Estados Unidos y empujando a algunos países europeos nuevamente a bloqueos.
Stephen Hoge , presidente de Moderna, ha dicho: "Vamos a tener una vacuna que puede detener el COVID-19".
El análisis intermedio de Moderna se basó en 95 contagios entre los participantes del ensayo que recibieron un placebo o la vacuna. De ellos, solo cinco infecciones ocurrieron en los que recibieron la vacuna, que se administra en dos inyecciones con 28 días de diferencia.
Una ventaja clave de la vacuna de Moderna es que no necesita almacenamiento ultrafrío como la de Pfizer, lo que facilita su distribución. Moderna espera que sea estable a temperaturas estándar del refrigerador de 2º a 8º durante 30 días y se puede almacenar hasta 6 meses a -20º.
La vacuna de Pfizer debe enviarse y almacenarse a menos 70º, el tipo de temperatura típica de un invierno antártico. A las temperaturas estándar del refrigerador, se puede almacenar hasta cinco días.
Los datos del ensayo de Moderna con 30.000 participantes también mostraron que la vacuna previno casos de COVID-19 graves, una pregunta que aún no se ha respondido con la vacuna de Pfizer,. De los 95 casos en el ensayo de Moderna, 11 fueron graves y los 11 ocurrieron entre los voluntarios que recibieron el placebo.
Moderna, parte del programa Operation Warp Speed ​​del gobierno de los EEUU, espera producir alrededor de 20 millones de dosis de la vacuna para EEUU este año, algunas de las cuales la compañía ya ha fabricado y está lista para enviar si recibe la autorización de la FDA.
Hoge , dijo: "Suponiendo que obtengamos una autorización de uso de emergencia, estaremos listos para enviar a través de Warp Speed ​​casi en horas".
DETALLES DE DATOS
Los 95 casos de COVID-19 incluyeron varios grupos clave que tienen un mayor riesgo de enfermedad grave, incluidos 15 casos en adultos de 65 años o más y 20 en participantes de grupos racialmente diversos.
La mayoría de los efectos secundarios fueron de leves a moderados. Sin embargo, una proporción significativa de voluntarios experimentó dolores y molestias más graves después de tomar la segunda dosis, incluido alrededor del 10% que tenía fatiga lo suficientemente grave como para interferir con las actividades diarias, mientras que otro 9% tenía dolores corporales graves. La mayoría de estas quejas fueron generalmente de corta duración, dijo la compañía.
Los datos de Moderna brindan una mayor validación de la plataforma de ARNm prometedora pero no probada previamente, que convierte al cuerpo humano en una fábrica de vacunas al persuadir a las células para que produzcan ciertas proteínas virales que el sistema inmunológico ve como una amenaza y contra las que monta una respuesta.
Moderna espera tener suficientes datos de seguridad requeridos para la autorización de EEU en la próxima semana y la compañía espera solicitar la autorización de uso de emergencia en las próximas semanas.
EEUU tiene la mayor cantidad conocida de casos y muertes de COVID-19 con más de 11 millones de infecciones y casi 250.000 muertes.
La Administración Trump se ha basado principalmente en el desarrollo de vacunas y tratamientos como respuesta a la pandemia. Moderna ha recibido casi mil millones de dólares en fondos para investigación y desarrollo del gobierno de los EE UU y tiene un acuerdo de 1,5 mil millones de dólares por 100 millones de dosis. El gobierno de EEUU también tiene la opción de recibir otros 400 millones de dosis.
La compañía espera tener entre 500 millones y mil millones de dosis en 2021, divididas entre sus distintas plantas de fabricación internacionales y de EEUU, dependiendo en parte de la demanda.
El gobierno de EEUU ha dicho que las vacunas COVID-19 se proporcionarán gratis a los estadounidenses, ya sea que tengan seguro médico, no estén asegurados o estén cubiertos por programas de salud gubernamentales como Medicare.
Moderna también dijo que utilizará sus datos para buscar autorización en Europa y otras regiones.
Otros países como China y Rusia ya han comenzado a vacunar. Rusia autorizó su vacuna COVID-19 “Sputnik-V” para uso doméstico en agosto antes de publicar datos de ensayos a gran escala. Dijo el 11 de noviembre que su vacuna tenía un 92% de efectividad en base a 20 infecciones en su gran ensayo.
REACCIÓN DE LOS MERCADOS
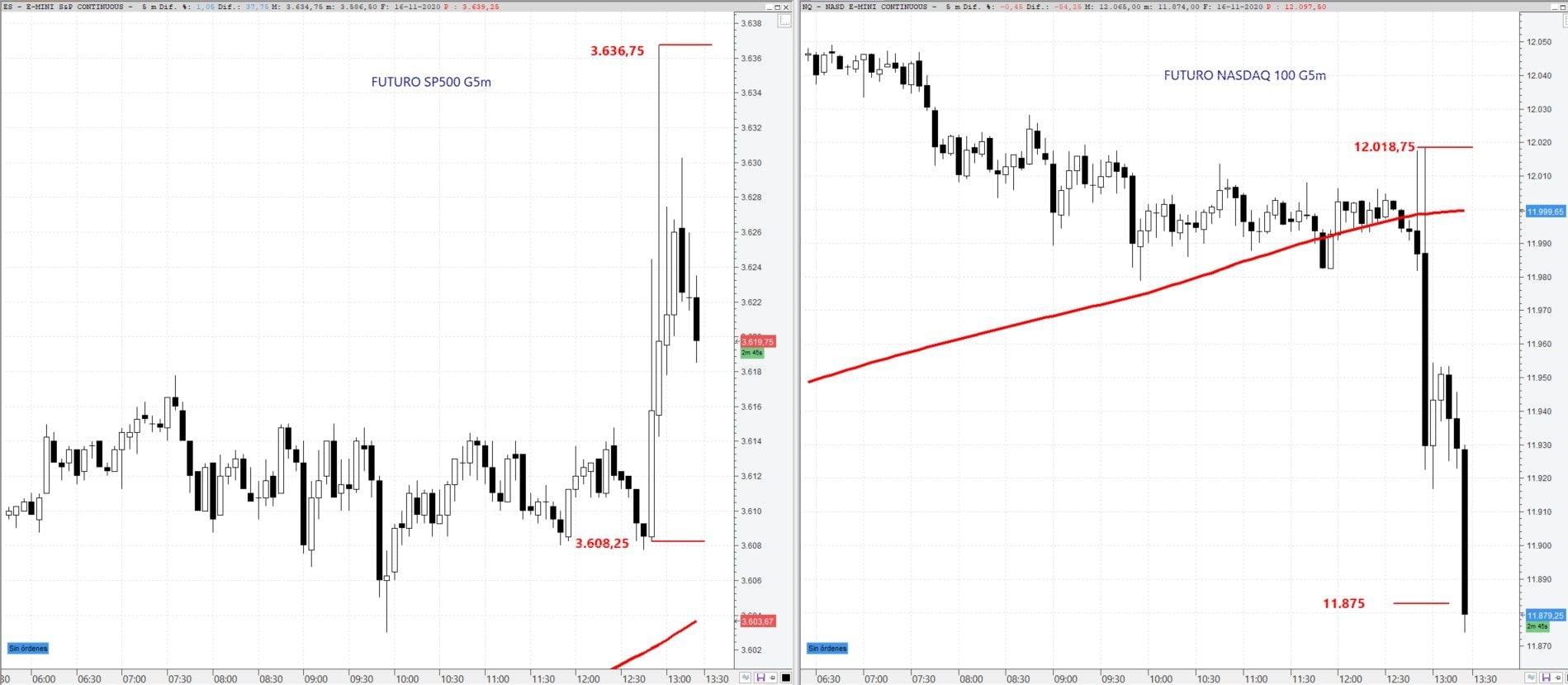
Los futuros del S&P 500 y NASDAQ 100 ha reaccionado de forma muy diferente a la noticia, una fuerte subida para el S&P 500 y una caída para el NASDAQ 100.
El IBEX 35 ha reaccionado rompiendo los 8.000 puntos. SI logra consolidarlos la recuperación del índice tiene el camino abierto.
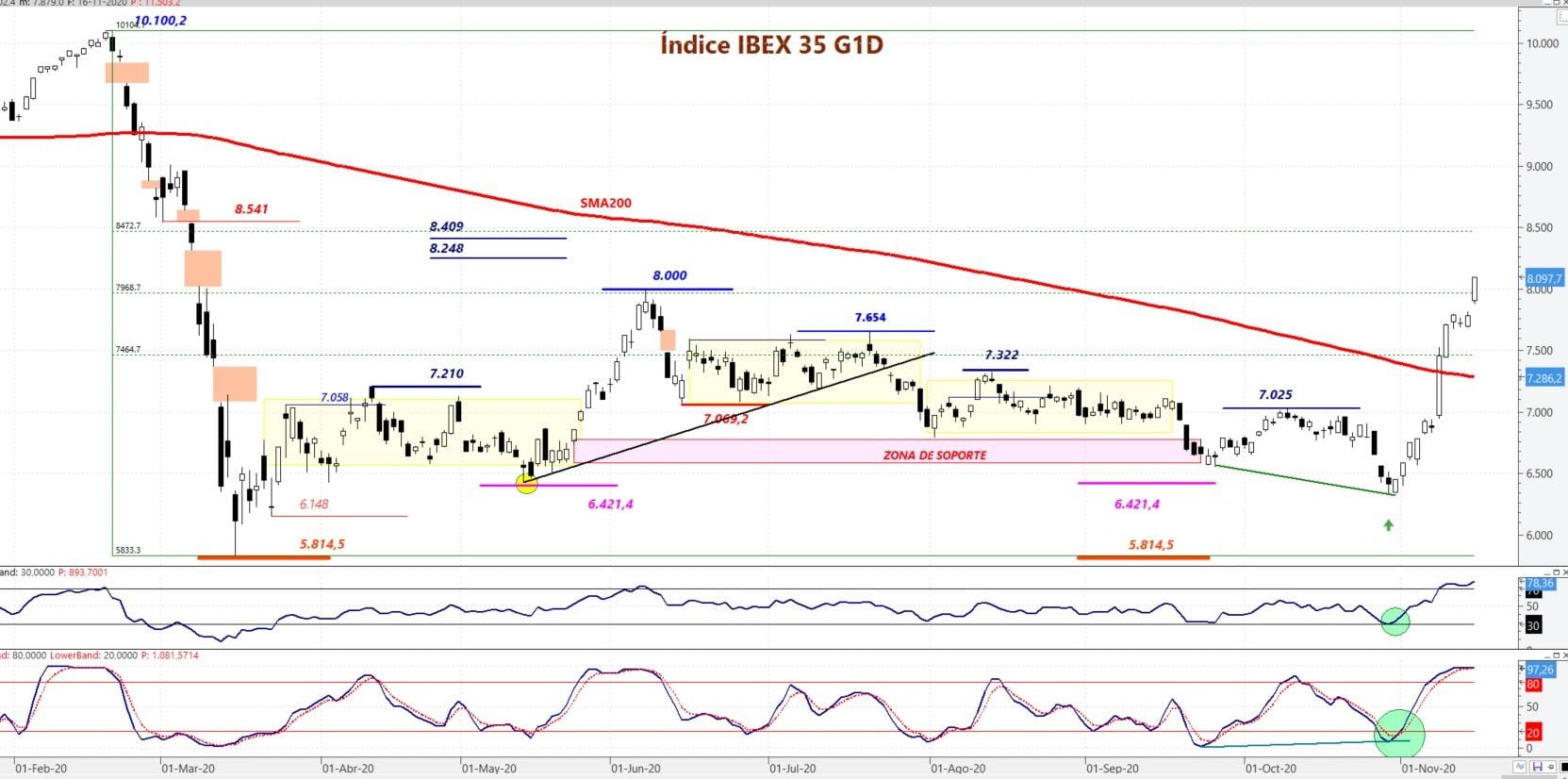
Ibex 35 rompe los 8.000 puntos. Gráfico diario
Reporte de Michael Erman y Julie Steenhuysen; Edición de Bill Berkrot, Caroline Humer, Peter Henderson y Edwina Gibbs. Traducción propia
Siga la actualidad de los mercados en La Bolsa Hoy
Programa práctico de estrategias de inversión y trading

